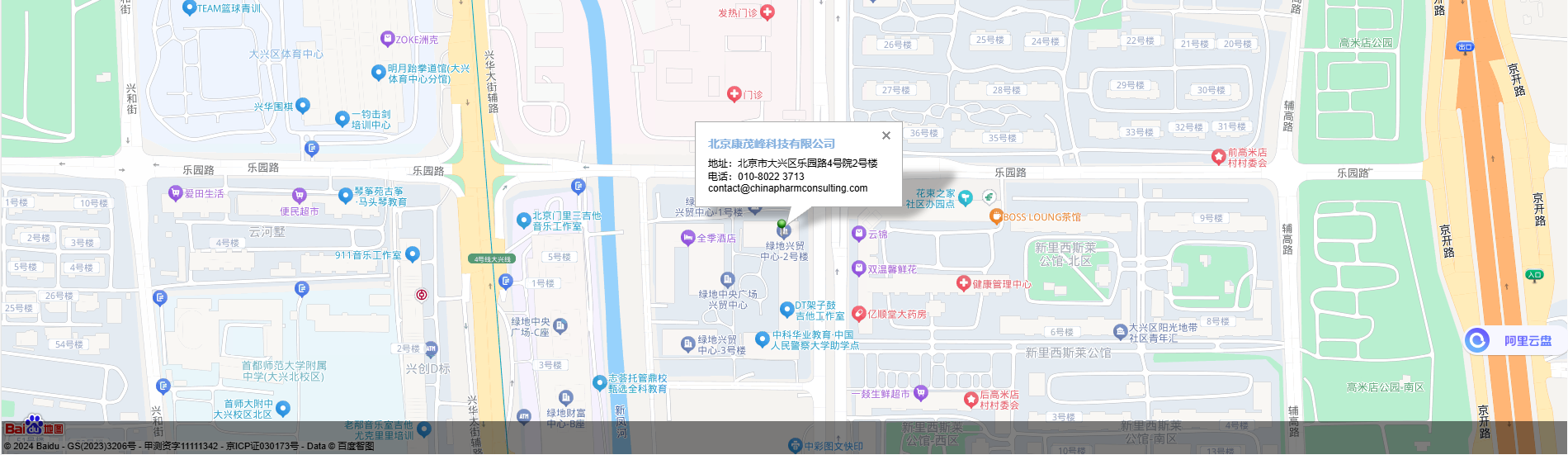
隨著我國對 ICH 指南適配的穩步進行,以及國家藥品監督管理局全面開展和推進藥品電子通用技術文檔(eCTD)申報通知的發布,藥品注冊申請的 eCTD 電子申報工作對醫藥企業申請人提出了一系列新的要求,申報資料 eCTD 相關法規、技術指南和規范標準內容繁多又復雜,在中國實施過程中,編寫、生成、驗證、提交、審評等環節都給申請人帶來極大的挑戰。
藥企注冊人對 CTD 的相關規范要求已然了熟于心,也許剛開始接觸 eCTD 時會認為不過是電子化的 CTD,但當真正著手操作時就會發現事情并沒有那么簡單。eCTD 并非只是將紙質文檔轉換成 PDF 文檔那么簡單,它還需要注冊人懂得計算機相關知識以及掌握一些必要的編輯軟件操作技能。而對于制藥企業來說,如果無法吃透法規,則不可避免地會影響正常申報效率。
北京康茂峰科技有限公司成立于 2002 年,專注進口藥品注冊資料翻譯,擁有一支行業知識淵博和專業技術精湛的 eCTD 服務團隊,早在 2018 年就開始為多家醫藥企業提供 eCTD 文件制作與排版工作,協助客戶完成了 IND、NDA、ANDA 等多個類型的藥品注冊申報。
康茂峰eCTD電子提交全流程
康茂峰熟知中國 eCTD 技術規范、行業指南與申報流程,于近期再次加大技術投入力度,部署了 eCTD 電子申報系統,為醫藥企業提供 eCTD 電子申報全流程服務,包含全套藥品注冊資料翻譯、格式排版并生成電子文件、eCTD 發布、eCTD 驗證、eCTD 遞交與存檔。
注冊資料翻譯
康茂峰作為中國成立最早的醫學翻譯公司之一,經二十年的創新發展,累積了億級醫學翻譯語料庫及數十萬條專業術語。擁有數十名專職醫藥及語言學專業譯員,年翻譯量超 5,000 萬字的翻譯能力,推動了康茂峰的藥品注冊資料翻譯能力位于行業前列。
文件準備
注冊資料翻譯完畢后,康茂峰 DTP 團隊會遵循藥審中心 eCTD 技術規范并結合客戶要求對 Word 文檔的字體字號、頁面布局、標題、段落進行 eCTD 格式調整。
根據不同客戶的格式要求,康茂峰 Office word 本身內嵌撰寫插件,自帶 CTD 格式模版,集成表格、圖標、目錄插入,常用化學符號、快捷序號生成、全文合規檢索等便捷功能,提高文檔格式合規性,大幅減少文檔準備時間。

Word 文檔排版完成后,使用 PDF 撰寫工具批量完成 Word 轉 PDF 后,根據客戶的工作規范或實際目錄對源文件建立書簽,對關鍵詞制作超鏈接。

康茂峰 eCTD 團隊會對全套 PDF 文檔進行 QC 質量檢測,核驗 PDF 文件屬性、安全性、字體、對應的書簽、目錄及鏈接,檢測鏈接沒有遺漏及目的頁跳轉正確,確保全部 PDF 文件合規性。
制作eCTD結構
根據 Tracking Log 的具體信息,使用 eCTD 發布器對編輯后的文件進行 M1 至 M5 的文件上傳,建立符合 eCTD 要求的框架結構。根據 Tracking Log 對葉元素標題及文件名進行編輯,確保文件名符合 eCTD 規范。在 eCTD 文件結構中制作跨文件鏈接,建立 M4、M5 模塊研究標記文件(STF),每個 STF 包括種屬、文件分類標簽、研究報告標題和其他文件修訂信息的文件、文件位置和順序信息。
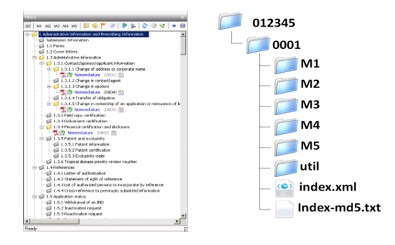
完成全部 eCTD 編輯出版后,再次進行 QA 質量檢測,包括對上傳文件及 eCTD 結構、相對路徑、添加或更新管理元數據、文件的元素標題及文件名等進行質量檢測。
eCTD出版驗證
依據中國 eCTD 驗證標準對出版的 eCTD 進行驗證,生成內容詳細、結構清晰的驗證報告,可準確定位至相關文件或內容,對驗證報告的錯誤提示進行解決修復,直到生成標準驗證符合 eCTD 結構規范的文件結構及 XML 文件。
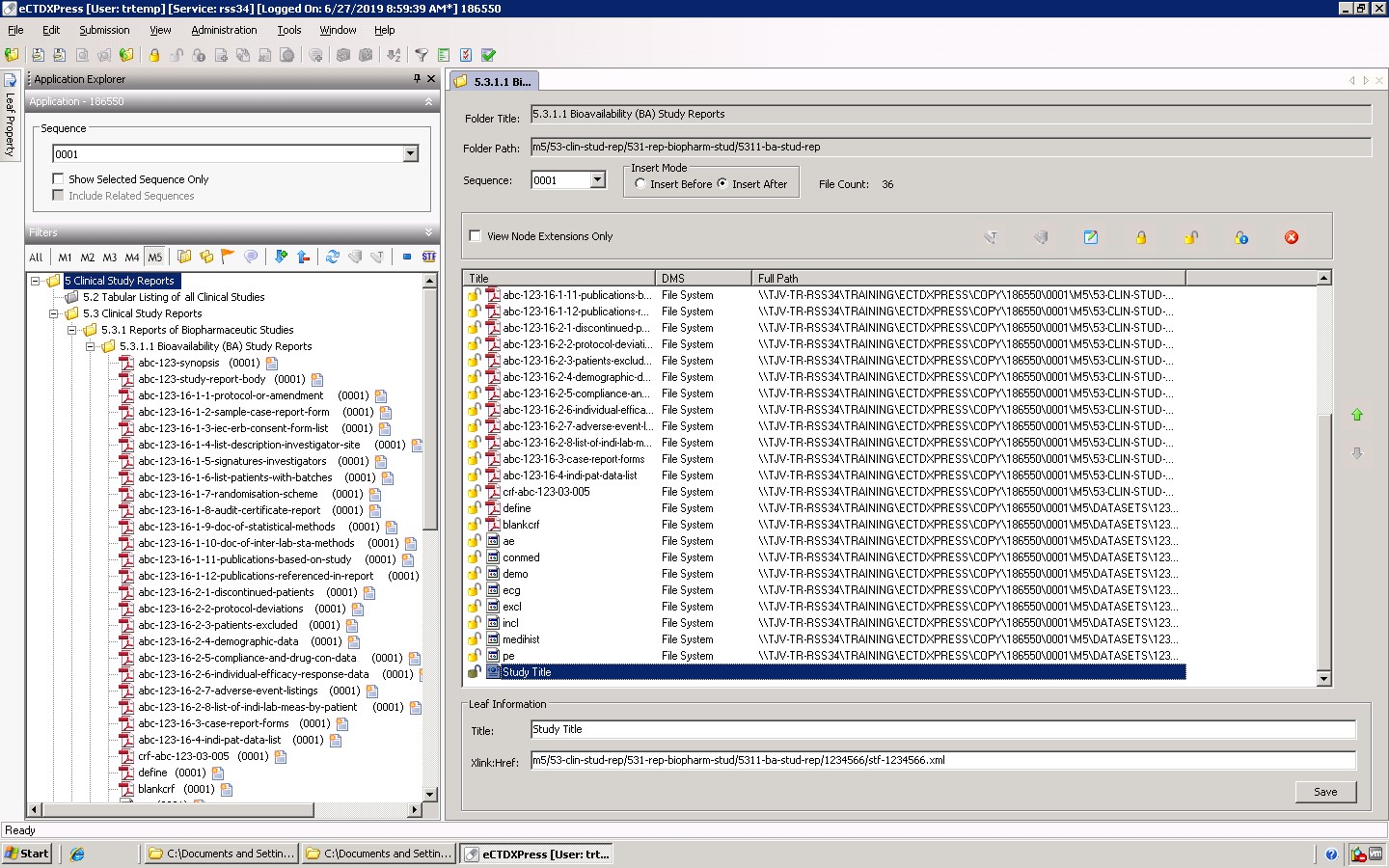
eCTD提交
用閱覽器以評審方視角審閱文章的內容合規,最終使用歸檔管理系統對 eCTD 文件進行歸檔刻錄光盤,最終將 eCTD 申報文件提交至監管機構。
由此可見,eCTD 電子提交不僅僅是將藥品申報文檔電子化,而是一個復雜的系統工程。
康茂峰 eCTD 電子申報系統及專業 eCTD 技術團隊可降低醫藥企業采購成本,助力醫藥企業加快藥品上市步伐。北京康茂峰科技有限公司總經理樊為國先生表示,作為醫學翻譯行業領導者,康茂峰在“為世界新藥進入中國提供專業指導和語言服務”使命指引下,以客戶為中心,匯聚行業智慧,致力為全球醫藥合作伙伴提供多元化、全方位的支持服務。